Suspensão ocorre porque lotes foram envasados em uma fábrica não aprovada
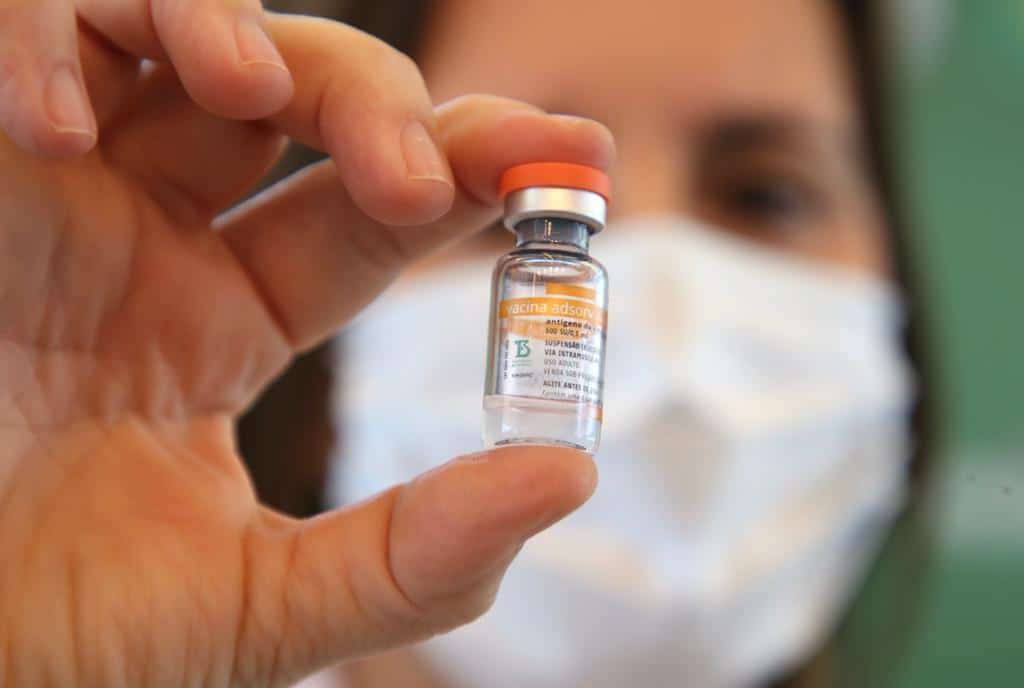
A Secretaria de Estado da Saúde (SES) informou na tarde deste sábado (4) que foi notificada da decisão da Agência Nacional de Vigilância Sanitária (Anvisa) em suspender, de forma cautelar, a distribuição e o uso de alguns lotes da vacina Coronavac/Butantan.
Diante da informação, a SES destaca iniciou o processo de notificação aos municípios sobre a suspensão da aplicação desse imunizante de acordo com os lotes recebidos. A orientação do Ministério da Saúde (MS) é que aqueles municípios que receberam os lotes citados suspendam a utilização dos mesmos e que mantenham as doses reservadas, conservando em temperatura entre 2ºC e 8º C até nova orientação do órgão federal.
Dos lotes suspendidos pela Anvisa, dois chegaram à Paraíba: o L202106038 (1 dose), recebido no mês de julho, e o 202107101H (2 doses), recebido no mês de setembro. A SES distribuiu um total de 13.220 doses.
“A SES aguarda orientação do Programa Nacional de Imunizações (PNI) à respeito da condução daquelas pessoas que podem ter sido vacinadas com as doses destes lotes”, disse a Pasta.
Segundo a Anvisa, a suspensão ocorre porque lotes foram envasados em uma fábrica não aprovada na autorização de uso emergencial da vacina. A medida foi publicada neste sábado em edição extra do Diário Oficial da União.
Em nota, a agência explicou que, nesse caso, “configura-se em produto não regularizado junto à Anvisa”, necessitando de atuação imediata para “mitigar um possível risco sanitário” à população.
Também em nota, o Instituto Butantan, que distribui a vacina no Brasil, esclareceu que a medida da Anvisa “não deve causar alarmismo”. “Foi o próprio instituto que, por compromisso com a transparência e por extrema precaução, comunicou o fato à agência, após atestar a qualidade das doses recebidas. Isso garante que os imunizantes são seguros para a população”, explicou.
De acordo com a Anvisa, o Instituto Butantan informou, ontem (3), que o laboratório chinês Sinovac, fabricante da CoronaVac, enviou ao Brasil vacinas envasadas em uma unidade que não foi inspecionada, nem aprovada pela agência brasileira. São 25 lotes com um total de 12.113.934 de doses do imunizante. Outros 17 lotes envasados no mesmo local, com 9 milhões de doses, estão em tramitação de envio e liberação ao Brasil.
A interdição cautelar tem o prazo de 90 dias. A Anvisa informou que, durante esse período, “trabalhará na avaliação das condições de boas práticas de fabricação da planta fabril não aprovada, no potencial impacto dessa alteração de local nos requisitos de qualidade, segurança e eficácia, e do eventual impacto para as pessoas que foram vacinadas com esse lote”.
Até o momento, segundo a agência, não há relatórios de inspeção emitidos por outras autoridades de referência, como o Esquema de Cooperação em Inspeção Farmacêutica (PIC/S) e a Organização Mundial de Saúde (OMS).
Certificação
Além disso, o Instituto Butantan deve regularizar o novo local na cadeia de fabricação da vacina. O órgão informou que, há 15 dias, encaminhou à Anvisa toda a documentação necessária para a certificação do processo de produção em que foram feitas as referidas doses. “Por isso, tem convicção que ela será concedida em breve. Caso necessário, pode complementar a solicitação com mais dados, inclusive da Sinovac, caso a agência julgue necessário”, explicou, reafirmando que todas as doses estão atestadas pelo rigoroso controle de qualidade do Butantan.
A Anvisa esclareceu que, na autorização de uso emergencial do imunizante, aprovada em 17 de janeiro deste ano, consta que as vacinas devem ser “importadas prontas da Sinovac, ou o granel da vacina formulada e estéril, sendo importado da Sinovac para envase e acondicionamento no Instituto Butantan. Entretanto, eventuais alterações nestas configurações devem passar por nova análise das áreas técnicas da Anvisa”.

Nenhum comentário:
Postar um comentário